Le mois de mai est le Mois de la sensibilisation à la santé mentale, un mouvement national visant à faire prendre conscience de l’importance de la santé mentale et des lacunes structurelles qui existent dans l’accès aux traitements et au soutien.
La santé mentale est au cœur du bien-être des personnes vivant avec le diabète de type 1 (DT1). C’est pourquoi, en 2021, Percée DT1 Canada a lancé sa Stratégie en santé mentale, dans le but de mieux soutenir la santé mentale des personnes atteintes de DT1, tout en poursuivant notre appui à la recherche de thérapies de guérison.
Le DT1 a des répercussions sur le bien-être émotionnel, social et mental tout au long de la vie, un ensemble que l’on désigne sous le nom de santé psychosociale. Les défis psychosociaux peuvent avoir un effet négatif sur les résultats liés au diabète, comme la glycémie. Plusieurs personnes vivant avec le DT1 souffrent de « détresse liée au diabète », un terme qui décrit l’impuissance, le stress, la culpabilité, l’inquiétude incessante et le déni qui viennent avec le diabète et le fardeau de l’autogestion des soins. De plus, les personnes vivant avec le DT1 sont plus à risque de souffrir de troubles de santé mentale, notamment de dépression, d’anxiété et de troubles de l’alimentation. Ces défis sont fréquents chez les personnes vivant avec le DT1 et peuvent être traités — mais ils sont souvent sous-estimés ou insuffisamment pris en charge en raison de lacunes dans les soins et le soutien.
Pour mieux répondre à ces besoins, Percée DT1 a défini une approche en trois volets pour sa Stratégie en santé mentale : 1) la production de connaissances par de nouvelles recherches; 2) un nouveau programme de formation destiné aux fournisseurs de soins de santé mentale; et 3) le développement de nouveaux soutiens communautaires. Depuis 2021, lorsque nous avons jeté les bases de cette stratégie, nous avons réalisé des progrès importants dans les trois domaines clés, grâce au soutien généreux des donateurs ainsi qu’à des partenariats avec le milieu universitaire, d’autres organisations liées au diabète et des collaborateurs communautaires.
Nous sommes heureux·ses de vous présenter les mises à jour apportées à ce programme au cours de la dernière année.
Mise à jour de la recherche
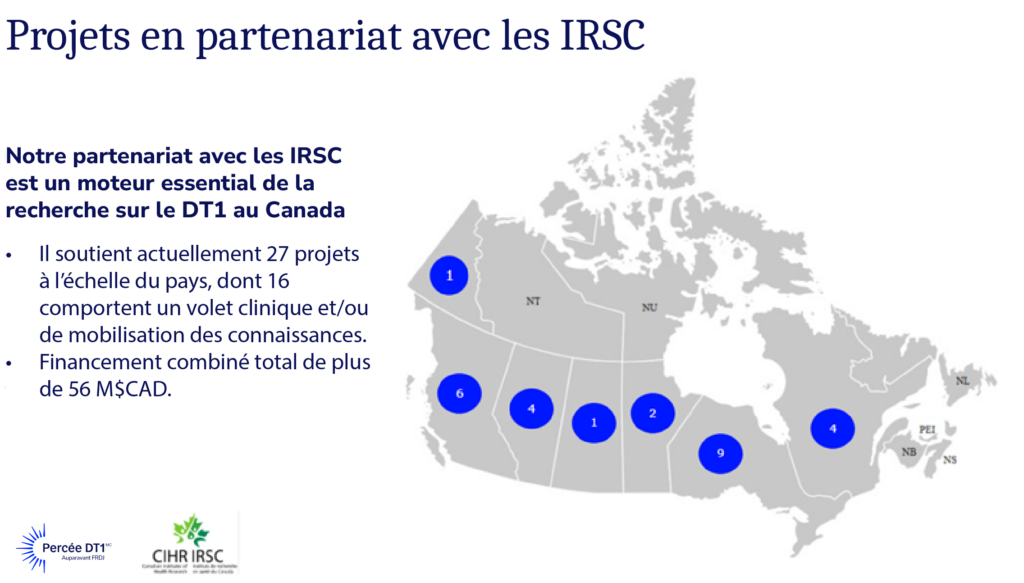
Depuis le lancement de notre Stratégie pour la santé mentale en 2021, nous avons investi 5 millions de dollars dans de nouvelles recherches axées sur le DT1 et la santé psychosociale, en collaboration avec des partenaires tels que la Fondation Brain Canada, les Instituts de recherche en santé du Canada (IRSC) et Michael Smith Health Research BC.
Cela comprend des fonds de Percée DT1 Canada, de la Fondation Brain Canada, des IRSC et de MSFHR.
9 prix au total :
- 3 avec la Fondation Brain Canada
- 4 avec les IRSC
- 1 prix d’impact (Percée DT1 uniquement)
- 1 prix en partenariat avec la Dre Tricia Tang (Michael Smith-Health Research BC)
Toutes les nouvelles recherches financées sont encore en cours. Conformément à notre stratégie de recherche mondiale dans ce domaine, qui vise à créer des programmes conçus pour être déployés à grande échelle et, à terme, aider un plus grand nombre de personnes, bon nombre des projets que nous soutenons portent sur le développement et la mise à l’essai d’interventions numériques. Par exemple, la Dre Tricia Tang et son équipe de l’Université de la Colombie-Britannique (UBC) ont mené une étude clinique sur leur plateforme de soutien virtuel par les pairs appelée REACHOUT. Cette plateforme utilise une application mobile pour offrir un soutien en santé mentale dirigé par des pairs, dispensé par des mentors formés, aux adultes vivant avec le DT1 dans les régions rurales et éloignées de la Colombie-Britannique. L’essai a évalué les effets du soutien par les pairs en mode virtuel sur des résultats tels que la détresse liée au diabète, la qualité de vie et l’HbA1c. Les travaux futurs porteront sur l’amélioration continue de la plateforme REACHOUT et l’élargissement de la portée des mentors formés afin que davantage de personnes vivant avec le DT1 puissent bénéficier de ce soutien.
D’autres études exploitant les technologies numériques pour mobiliser les personnes vivant avec le DT1 à travers le Canada comprennent celle de la Dre Deborah Da Costa, de l’Université McGill, dont l’étude teste les meilleures façons de soutenir la santé mentale et le bien-être des femmes atteintes de diabète pendant la grossesse, ainsi que celle de la Dre Holly Witteman, de l’Université Laval, qui développe un réseau de soutien par les pairs en ligne destiné aux personnes vivant avec le DT1 ayant des besoins et des intérêts particuliers.
D’autres recherches soutenues par Percée DT1 visent à améliorer les résultats liés à la transition des soins pédiatriques aux soins pour adultes — une étape de vie durant laquelle de nombreux jeunes cessent de consulter leur endocrinologue, ce qui peut entraîner des difficultés comme une hausse de l’HbA1c, de l’isolement, de la stigmatisation et des troubles de l’alimentation. La Dre Sonia Butalia, de l’Université de Calgary, mène un essai clinique sur un système conçu pour améliorer cette transition, qui a permis une amélioration de la glycémie chez les participant·e·s au projet pilote initial à Calgary. Dans le cadre du plus récent essai financé par Percée DT1 et les IRSC, le programme — qui repose sur une coordonnatrice de la transition et des communications soigneusement élaborées — est étendu à d’autres établissements des Services de santé de l’Alberta (AHS) à Calgary, Edmonton, Lethbridge, Medicine Hat et Red Deer.
Ces cliniques et partenaires communautaires sont très enthousiastes face aux travaux de l’équipe sur la transition, et les Services de santé de l’Alberta (AHS) ont approuvé le budget nécessaire pour que le projet se poursuive au-delà de la durée de la subvention. Le déploiement de ce modèle de soins permettrait à ce groupe démographique de personnes vivant avec le DT1 de ne plus passer entre les mailles du filet lors de la transition des soins pédiatriques aux soins pour adultes.
« Mon fils Luke vit avec le DT1 depuis l’âge de 5 ans, et il est maintenant adolescent. Cela a été un grand défi pour lui et pour toute notre famille, et même si Luke bénéficie d’un bon soutien — en grande partie grâce à son implication auprès de Percée DT1 — l’adolescence et le début de l’âge adulte présentent leur propre lot de défis. Je suis tellement reconnaissant que la Dre Butalia et son équipe mettent en œuvre un modèle de soins pour les jeunes en transition qui, je l’espère, pourra aider Luke d’ici quelques années. C’est formidable de voir cette recherche essentielle être déployée à grande échelle en Alberta, et, idéalement, à travers tout le pays. » – Ryan MacDonald, Calgary, coprésident de la Campagne pour accélérer de 100 millions $ de Percée DT1.
Programme de formation Santé mentale + Diabète
De nombreuses personnes vivant avec le DT1 font face à des défis en santé mentale qui nécessitent le soutien d’un·e professionnel·le de la santé mentale agréé·e — idéalement quelqu’un qui comprend les défis uniques que le diabète pose à la santé mentale. Pour aider à sensibiliser les fournisseurs de soins de santé mentale au Canada à cette réalité, Percée DT1 a lancé le programme de formation Santé mentale + Diabète au début de 2023, en collaboration avec Diabète Canada.
Ce cours entièrement bilingue est offert virtuellement en deux volets : un pour les fournisseurs de soins de santé mentale agréés au Canada (qui comprend une séance en direct axée sur les compétences cliniques) et un autre, destiné aux autres fournisseurs de soins de santé et au grand public, composé uniquement de modules autodirigés. Ce programme est offert gratuitement, donne droit à 10 crédits de formation continue pour certains fournisseurs, et est approuvé par la Société canadienne de psychologie ainsi que par d’autres associations.
En mai 2025, plus de 500 fournisseurs de soins de santé mentale avaient déjà terminé le programme, et plus de 1 000 autres personnes (autres types de fournisseurs de soins de santé ou membres de la communauté du DT1) s’y étaient inscrites. Les premiers résultats sur les retombées du programme de formation ont récemment été publiés dans une revue scientifique avec comité de lecture, le Journal canadien du diabète. Une autre étude d’évaluation est en cours pour mesurer l’impact du programme sur la pratique clinique des participant·e·s.
Développement des soutiens communautaires
La communauté du DT1 est diversifiée et comprend de nombreux sous-groupes dont les besoins et les défis psychosociaux varient. Afin de répondre à ces besoins, au cours des trois premières années de notre stratégie, nous avons travaillé à développer des soutiens communautaires par le biais de diverses initiatives, avec l’appui de notre dévoué Conseil consultatif sur la santé mentale — un groupe de plus de 100 bénévoles ayant une expérience vécue diversifiée du DT1. Au cours de la dernière année, nous avons poursuivi l’élargissement de nos sources de soutien communautaire de plusieurs façons.
Tout d’abord, nous avons organisé plusieurs événements virtuels pour mobiliser et sensibiliser notre communauté :
- Plus de 500 personnes ont assisté à nos séances Santé mentale et DT1 dans le cadre de la Série éducative Percée DT1 en mai 2024 (en anglais et en français).
- Près de 200 professionnel·le·s de la santé ont participé à des séances sur le DT1 et les troubles de l’alimentation (en anglais et en français), organisées en collaboration avec le National Eating Disorder Information Centre (NEDIC). Ces webinaires ont permis de favoriser le dialogue et les occasions d’apprentissage pour les fournisseurs de soins de santé et d’autres membres de la communauté.
- Plus de 500 personnes ont assisté à nos séances Troubles de l’alimentation et DT1, également dans le cadre de la Série éducative Percée DT1. Ces événements bilingues mettaient en vedette des intervenant·e·s de NEDIC, d’ANEB (Anorexie et boulimie Québec), ainsi que des personnes ayant une expérience vécue. On y a exploré les réalités et les défis de la gestion des troubles de l’alimentation liés au DT1. En favorisant le dialogue autour de ce sujet sous-estimé, nous espérons que les troubles de l’alimentation seront mieux reconnus et traités, menant ainsi à de meilleurs soins et résultats pour les personnes concernées.
Ensuite, nous avons élargi notre Répertoire de fournisseurs de soins de santé mentale formés au diabète grâce à notre nouveau programme de formation. Ce répertoire constitue une ressource précieuse pour les personnes vivant avec le diabète ou les équipes de soins souhaitant entrer en contact avec un fournisseur de soins de santé mentale sensibilisé à leur réalité. En mai 2025, plus de 180 fournisseurs de partout au Canada y étaient inscrits, et ce nombre devrait continuer de croître à mesure que de nouveaux fournisseurs suivent la formation.
Troisièmement, nous avons suivi l’évolution et soutenu la réussite des projets financés dans le cadre de notre tout premier programme de subventions communautaires Santé mentale et DT1 — un mécanisme destiné à stimuler les efforts d’autres organisations qui développent de nouveaux programmes communautaires pour soutenir la santé mentale et le bien-être dans la communauté du DT1. Les premières subventions accordées dans le cadre de ce programme progressent bien dans leur mandat de 18 mois, et des mises à jour seront partagées à la fin de 2025.
Enfin, nous avons le plaisir de vous présenter une nouvelle série de vidéos pour partager les histoires de notre communauté : Au-delà des chiffres : De vraies histoires sur la santé mentale avec le DT1. Nous diffuserons ces vidéos tout au long du Mois de la sensibilisation à la santé mentale et au-delà afin de contribuer à normaliser les problèmes psychosociaux, les solutions et les victoires qui font partie du quotidien avec le DT1. Cette série de 20 vidéos aborde les thèmes des relations et du soutien social, des transitions de vie, ainsi que de l’adaptation et de la résilience.
Merci à notre communauté
Percée DT1 Canada demeure extrêmement reconnaissante du soutien de son Conseil consultatif sur la santé mentale, de ses bénévoles clés et de ses partenaires philanthropiques, notamment les partenaires financiers tels que la Fondation Brain Canada et Diabète Canada, sans qui nos progrès dans ce domaine n’auraient pas été possibles.
Pour en savoir plus sur les soutiens en santé mentale, veuillez consulter le Répertoire à l’adresse repertoire.perceeDT1.ca ou visiter notre page de ressources en santé mentale.
Ressources et événements de la communauté du DT1
Ressources web et blogues